5. ИЗОМЕРИЯ КОМПОНЕНТОВ ЭФИРНЫХ МАСЕЛ
Многие вещества, входящие в состав эфирных масел, имеют одну и ту же общую химическую формулу (называемой брутто-формулой). Например, среди веществ с формулой С10Н16 существуют сотни веществ, принадлежащих к самым различным химическим классам, обладающих различными физическими и химическими свойствами. Некоторые вещества с такой формулой - твердые при комнатной температуре вещества, другие – жидкие. Одни химически устойчивы, другие быстро разлагаются или окисляются. Такое явление называется изомерией. Существуют различные типы изомерии. Среди них главными являются структурная, геометрическая, пространственная и оптическая.
Структурные изомеры (изомеры положения) — это изомеры с разной последовательностью связанных атомов. Простейшим примером структурной изомерии являются вещества бутен-1 (Н2С=СН–СН2–СН3) и бутен-2 (Н3С–СН=СН–СН3). Цифрой в названии вещества обозначается атом углерода, у которого располагается двойная связь.
В классе терпеновых углеводородов с брутто-формулой С10Н16 существует несколько сотен структурных изомеров. Причина такого многообразия в том, что одно и то ж количество атомов углерода могут соединяться друг с другом различным сочетанием и образовывать прямые, разветвленные и замкнутые цепи.
В начале девятнадцатого веке, когда химики стали работать над выделением монотерпеновых углеводородов из природных источников с целью их дальнейшего изучения, еще не существовало единой системы названий химических веществ. Вещества называли по источнику их происхождения (система тривиальных названий). Например, из эфирного масла сосны (родовое название Pinus) был выделен бициклический терпен, который имел общую формулу С10Н16. Это вещество назвали «пинен».
Трудности с названиями стали возникать, когда стало понятно, что «пинен» не является индивидуальным веществом, а представляет собой смесь веществ с одной и той же формулой. Поэтому было предложено назвать эти вещества α- и β-пиненами. Впоследствии появились названия других терпенов: α- и β-фелландрен, α-, β- и γ-терпинен и т.д. Приставки α-, β-, γ- и т. д. обозначают положение двойных связей в молекуле этих[ веществ. Все эти вещества являются изомерами с одной и той же брутто-формулой. Несмотря на это они сильно различаются по химическим и физическим свойствам.
Вещества α-пинен и β-пинен входят в состав многих эфирных масел и оказывают разное физиологическое действие. α-Пинен входит в состав более 400 эфирных масел, особенно велико его содержание в эфирных маслах сосен и можжевеловых деревьев. В эфирном масле хвои можжевельника содержится до 70% α-пинена, в эфирном масле ягод можжевельника — до 25%, в эфирном масле корней дягиля — около 24%. β-Пинен часто встречается одновременно с α-пиненом. Велико содержание β-пинена в эфирных маслах сосновых. В эфирном масле лимона его содержится до 5-15%%. Это вещество было также найдено в эфирном масле тысячелистника и шалфея.
При переходе к окисленным формам монотерпенов, имеющих общую формулу С10Н18О, количество изомеров возрастает до нескольких тысяч. Так же, как и в случае с монотерпенами, им давали имена по источнику, из которого они были впервые выделены. Так возникли названия линалоол (выделен из линалоэ), гераниол (из герани), цитронеллол (из цитронеллы) и т. д.
В классе сесквитерпеновых углеводородов с брутто-формулой С15Н24 и их окисленных форм С10Н26О число возможных изомеров вырастает многократно. Конечно, в природных условиях встречаются далеко не все соединения, но их число составляет многие тысячи!
Все эти вещества обладают самым широким спектром биологического действия, и даже самые близкие изомеры имеют свойства, резко отличающиеся друг от друга.
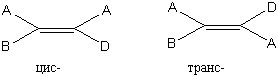
Геометрические изомеры (также называемые цис- и транс-изомерами) имеют разную ориентацию групп относительно двойной связи, которая присутствует во всех терпеновых соединениях. Цис-изомерами называют геометрические изомеры, у которых заместители лежат по одну сторону от плоскости двойной связи, у транс-изомеров заместители располагаются по разные стороны от плоскости двойной связи.

Примерами геометрических изомеров являются вещества цис-3-гексенол и транс-3-гексенол, которые присутствуют в траве и имеют хорошо знакомый нам запах свежескошенной травы.
Поскольку в терпеновых соединениях всегда присутствуют двойные связи, то во многих случаях даже при полной структурной идентичности они существуют в виде цис- и транс-изомеров. Монотерпеновые спирты нерол и гераниол имеют совершенно одинаковое химическое строение (3,7-диметил-2,6-октадиен-1-ол), за тем исключением, что часть молекулы, содержащая гидроксильную группу, повернута вокруг двойной связи на 1800.
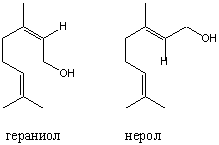
При этом нерол является цис-изомером (цис-3,7-диметил-2,6-октадиен-1-ол), а гераниол — транс-изомером (транс-3,7-диметил-2,6-октадиен-1-ол). Химические свойства нерола и гераниола схожи между собой, но нерол обладает очень чистым запахом розы, тогда как запах гераниола более грубый.
Еще одним примером геометрических изомеров является анетол, составляющий до 90% эфирного масла анисового семени. Анетол представляет собой смесь цис- и транс-изомеров. Транс-анетол является широко распространенным ароматизатором и имеет низкий уровень токсичности, тогда как цис-анетол очень токсичен. К счастью, доля цис-анетола в эфирных маслах очень невелика, поэтому при умеренном ее использовании она не представляет опасности для здоровья. Однако при старении эфирных масел, особенно при воздействии света, уровень содержания цис-формы может увеличиваться. Эта информация может иметь интерес для тех, кто предпочитает напитки «Перно» или «Узо», содержащие анетол!
Иногда цис- и транс-изомеры (очень редко, в виде исключения) называют с использованием букв греческого алфавита. Так, в случае азарона (основного компонента эфирные масла аира европейского происхождения) его транс-изомер (транс-азарон) называют просто «азарон», а цис-изомер получил название β-азарон (который содержится, главным образом, в составе эфирные масла индийского происхождения). β-азарон (в отличие от азарона) обладает сильным абортивным, аллергическим и канцерогенным действием.
Структурные и геометрические изомеры отличаются друг от друга физико-химическими и биологическими свойствами. Они легко отделяются друг от друга различными методами (например, методами хроматографии).
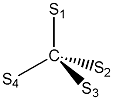
Пространственными изомерами (стереоизомерами) называют изомеры с одинаковой последовательностью атомов, но разной ориентацией в пространстве вокруг так называемого ассиметричного атома углерода. Ассиметричный атом углерода определяют как атом углерода (C), который связан с четырьмя различными заместителями (S1, S2, S3, S4). Два заместителя (S1 и S2) находятся в одной плоскости с атомом углерода и соединяются с ним связью, которая обозначается обычной чертой. Два других заместителя (S2 и S3) находятся с атомом углерода в другой плоскости (перпендикулярно первой) и соединяются с ним связями, которые обозначают специальными черточками. Прерывистая черточка, соединяющая атом углерода и заместитель S2 указывает на то, что связь C-S2 уходит от нас за плоскость листа. Жирная черточка, соединяющая атом углерода и заместитель S3 указывает на то, что связь C-S3 выступает над плоскостью листа. Такая система обозначений используется для графического изображения формул различных стереоизомеров.
При этом различают два типа пространственной изомерии. Одни стереоизомеры могут в пространстве быть зеркально симметричны, другие таковыми не являются.
Стереоизомеры, которые имеют ассиметричный атом углерода, но не способны быть зеркальными изображениями друг друга, называются диастереомерами. В качестве примера можно привести борнеол, существующий в природе в виде собственно борнеола (I) и его диастереомера изоборнеола (II), который очень редко и небольшом количестве присутствует в натуральных эфирных маслах.
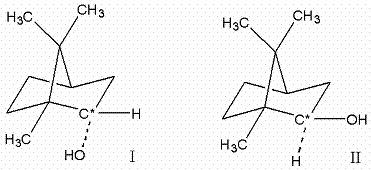
Оба соединения имеют одинаковое строение, но частично различаются пространственным расположением атомов, т. е. являются стереоизомерами. Ассиметричный атом углерода обозначен звездочкой. Как видно из структурных формул, к этому атому присоединено четыре разных заместителя: группа OH, группа H, а также две различные части углеродного кольца с шестью атомами. Но они не являются зеркальными изомерами, так как расстояния между некоторыми атомами у двух веществ отличаются. Видно, что группа OH у борнеола расположена значительно ближе к группе CH3, чем у изоборнеола.
Различные расстояния между соответствующими группами в диастереомерах обуславливают различия в физических и химических свойствах. Например, борнеол плавится при 209°С, в то время как температура плавления изоборнеола 214°С. Запах борнеола очень приятный, освежающий, напоминает хвою, в то время как изоборнеол имеет камфорный («целлулоидный») запах. Указанные различия важны, поскольку синтетически получаемый изоборнеол и его ацетат - изоборнилацетат - добавляют в эфирные масла, содержащие недостаточное количество собственного борнеола и борнилацетата. Таким образом, например, корректируют состав эфирного масла пихты, однако такое «скорректированное» эфирное масло будет иметь в запахе посторонний камфорный тон.
Еще одним примером стереоизомеров является ментол — основной компонент мятного масла. Особенность химического строения ментола в том, что у него не один ассиметричный центр, а два. Это приводит к тому, что ментол существует уже в четырех диастереомерных формах. Все они присутствуют в эфирные масла перечной мяты. Главный изомер – собственно ментол составляет до 95% смеси изомеров, его другая форма – неоментол составляет 2–5%. Остальные диастереомерные формы ментола (изоментол и неоизоментол) присутствуют в небольшом количестве (0,1-0,2%). Как и в случае борнеола, все формы ментола отличаются физико-химическими свойствами и легко отделяются друг от друга.
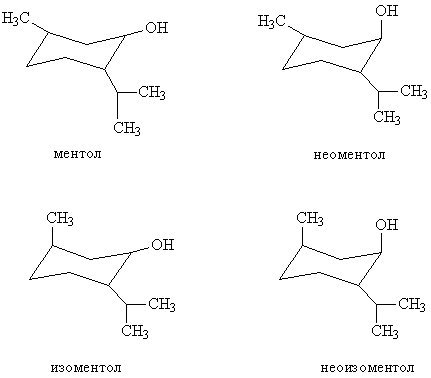
Диастереомерные формы ментола.
После того, как были найдены разновидности мяты (иногда их называют японскими или индийскими), содержащие до 80% ментола, их стали использовать для извлечения ментола вымораживанием. Полученный ментол используют в пищевой промышленности и в медицине для ароматизации лекарственных форм. Остальные диастереомерные формы ментола не вымораживаются, так как имеет температуру замерзания (кристаллизации) очень низкую. Остаток эфирного масла, хотя и содержит 30-40% ментола, не является полноценным заменителем классической перечной мяты, так как у нее неприятный запах травянисто-землистого направления из-за повышенного содержания неоментола и изоментола. Методом хроматографии эти изомеры легко обнаружить и уличить поставщика такой мяты в фальсификации.
Стереоизомеры, которые имеют ассиметричный атом углерода и являются зеркальными отображениями друг друга, называются энантиомерами.
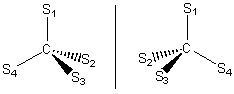
Энантиомеры.
Такие стереоизомеры примечательны тем, что одна форма вращает плоскость поляризованного света направо, а другая — налево. Такое свойство веществ называется оптической активностью, а такие изомеры называются оптическими изомерами.
Плоско поляризованный свет – это световой луч, который специальным методом сформирован (вырезан) из объемного светового потока таким образом, чтобы он представлял собой плоскость, в которой происходят колебания электромагнитных (световых) волн. Вращение плоскости поляризации – это изменение угла плоскости колебания электромагнитных (световых) волн после прохождения через вещество.
Если от наблюдателя, к которому направлен свет, проходящий через оптически активное вещество, вращение плоскости поляризации происходит вправо (по движению часовой стрелки), то вещество называют правовращающим, и перед его названием ставят индекс «d» или знак «(+)» [(+)-линалоол или d-линалоол]. Если же вращение плоскости поляризации происходит влево (против часовой стрелки), то вещество называют левовращающим, и перед названием ставят индекс «l» или знак «(-)» [(-)-линалоол или l-линалоол].
Эти две формы, вращающие свет направо и налево, называются, соответственно, право- и лево-вращающими или «хиральными» формами. Слово «хиральный» происходит от греческого «хиро» что означает «рука». Своеобразными примерами хиральных объектов являются руки, ноги, обувь и перчатки, правые и левые форм, которых являются зеркальными отражениями и их невозможно наложить одно на другое, не выходя из плоскости.
Смесь двух энантиомеров в равных количествах называют рацемической смесью, и она будет иметь нулевое оптическое вращение, так как вращательные эффекты (правый и левый) уравновесятся.
В природных продуктах очень часто существует только одна из этих форм. Правовращающий лимонен (d-лимонен, (+)-лимонен) найден в эфирном масле апельсина, лимона, мандарина, лайма, грейпфрута, бергамота, нероли, петигрейна, элеми, тмина, укропа, фенхеля, петрушки, эригерона, ортодона. Левовращающий лимонен (l-лимонен, (-)-лимонен) найден в эфирном масле хвойных, пихт, звездчатого аниса, перечной мяты, сперминта, кайепута.
В соответствии с новой номенклатурой, направление вращения обозначается, например, для лимонена, как (R)-(+)-лимонен (правовращающий лимонен) и (S)-(-)-лимонен (левовращающий лимонен).
При наличии нескольких асимметричных атомов углерода, в молекуле появляется большое количество возможных изомерных форм. Например, ментол имеет три ассиметричных атома углерода. Один из оптических изомеров ментола обозначается как (1R,3R,4S)-(-)-ментол. Это означает, что в положении 1 и 3 в молекуле ментола оптическое вращение правое, в положении 4 - левое, а общее (результирующее) вращение - левое.
Каждая из четырех диастереомерных форм ментола (см. выше) может существовать в двух оптически активных (энантиомерных) формах. Таким образом, в эфирном масле мяты ментолу соответствует 8 изомеров, обладающих разными свойствами.
С химической точки зрения оптические изомеры являются совершенно идентичными веществами. Тем не менее, этот вид изомерии играет исключительную роль в эфирных маслах. Оптические изомеры одного и того же вещества почти всегда сильно различаются как качеством, так и силой запаха. Чаще всего левовращающие изомеры обладают более сильным ароматом (иногда правовращающие изомеры вообще не имеют запах), их запах богаче оттенками, качество запаха левовращающих изомеров воспринимается как более приемлемое. Именно уникальное для каждой эфирные масла сочетание правовращающих и левовращающих форм веществ создает тот природный аромат, который так ценится в высококачественной парфюмерии.
Оптическая изомерия имеет большое значение при оценке качества ароматных веществ. В некоторых случаях (например, у камфоры) различия в запахе между (+)- и (-)-изомерами нет. Вещество (+)-нуткатон имеет характерный горьковатый запах грейпфрут, которого не наблюдается у (+)-нуткатона. Оптически активные вещества интересны также тем, что пороговое значение (самая маленькая концентрация, при которой соединение можно распознать по запаху) восприятия запаха для изомеров сильно различается. Например, для (+)-нуткатона оно составляет 0,001 мг/л, в то время как для (-)-нуткатона это величина равняется 1,0 мг/л.
Для ароматерапии важной особенностью оптических изомеров является их различное физиологическое действие на организм человека. Оптические изомеры одного и того же вещества отличаются друг от друга биологическим действием. Биологическая активность левовращающих изомеров часто сильнее правовращающих. Например, многие лекарственные средства, полученные синтетически и способные существовать в виде оптических изомеров, обладают биологической активностью только в виде левовращающего изомера. Оптически активное лекарственное средство левометицин обладает биологической активностью только в левовращающей форме и не активно в правовращающей. Более того, пример талидомида, снотворного для беременных, показал, что один из его оптических изомеров (от которого «забыли» очистить этот медицинский препарат) оказывает сильное негативное влияние на развитие плода.
В эфирном масле ромашки лекарственной содержится (-)-α-бисаболол, который обладает сильным противовоспалительным действием. В тоже самое время (+)-α-бисаболол, выделенный из тополя бальзамического (Populus balasamifera), и (±)-бисаболол (рацемат, полученный синтетически) обладают значительно меньшим противовоспалительным действием.
Другим примером являются оптические изомеры карвона: (+)-карвон, содержащийся в эфирном масле тмина, относят к категории токсичных веществ, тогда как (-)-карвон, входящий в состав эфирном масле перечной мяты, практически не обладает токсическими свойствами. Таких примеров множество.
Различия во вкусе, запахе и фармакологических свойствах оптических изомеров объясняются их неодинаковым взаимодействием с диссимметричными (обладающим лишь одним направлением вращения) ферментативными и рецепторными системами в организме человека.
Химически разделить оптические формы невозможно, поэтому для их разделения используют физические методы, например, фракционную кристаллографию. Впервые этим методом Пастер разделил винные кислоты. Он обратил внимание, что кристаллы винной кислоты имеют разную форму. Используя пинцет и микроскоп, Пастер рассортировал эти кристаллы по внешнему виду. Впоследствии оказалось, что эти две группы кристаллов обладают противоположным оптическим вращением.
Современным аналитическим способом разделения энантиомеров является хроматография на специальных «хиральных» (оптически активных) колонках.
Многие компоненты эфирных масел обладают оптической активностью, при этом компоненты, обладающие левым вращением, компенсируют правое вращение других компонентов. В результате такого смешения эфирное масло обладает результирующим оптическим вращением, которое называется оптическим вращением эфирного масла.
Для каждого эфирного масла существует стандартное (нормальное) соотношение энантиомеров. Например, в норме в эфирном масле лавра (Laurus nobilis) содержится 80% (-)-α-терпинеола и 20% (+)-α-терпинеола. Процентное соотношение двух энантиомеров одного вещества называется оптической чистотой. Однако неправильно думать, что если эфирные масла содержат в своем составе один определенный энантиомер или если в ней будет найден энантиомер низкой оптической чистоты (то есть состоит из лево- и правовращающих форм), то она фальсифицирована. Среди природных веществ имеется большое количество рацемических смесей изомеров (т. е. право- и лево-вращающие изомеры присутствуют в смеси в соотношении 50:50, поэтому такие компоненты не вносят вклад в оптическое вращение эфирного масла в целом). Рацемизация может происходить во время дистилляции с водяным паром. Так, при экстракции герани холодным диэтиловым эфиром в полученном эфирном масле (абсолю) будет содержаться 64,4% (S)(+)-изомера линалоола. При дистилляции с водяным паром получается рацемическая смесь изомеров линалоола. Таким образом, энантиомерная чистота не является абсолютным показателем натуральности эфирного масла.
Не все изомеры оптически активны, а у многих величина оптического вращения очень невелика. Тем не менее, с помощью этого явления можно определить чистоту эфирного масла. Синтетические ароматизаторы часто (но не всегда!) оптически неактивны. При их добавлении природное оптическое вращение сфальсифицированного эфирного масла будет иметь значения, отличающиеся от показателей натуральной эфирного масла. Более того, входящие в синтетический рацемат оптические формы могут оказывать непредсказуемое и опасное действие на живой организм.